Wasserstoff: Unterschied zwischen den Versionen
| Zeile 42: | Zeile 42: | ||
Die einfachste Labormethode zur Erzeugung kleiner Mengen Wasserstoff: | Die einfachste Labormethode zur Erzeugung kleiner Mengen Wasserstoff: | ||
| − | Die Reaktionsgleichung: | + | '''Die Reaktionsgleichung:''' |
Zn + 2HCl = ZnCl_2 + H_2 | Zn + 2HCl = ZnCl_2 + H_2 | ||
Version vom 29. April 2026, 08:17 Uhr
Inhaltsverzeichnis
Siehe auch:
Der kleine Alchemist ├─ Wasser – Grundlagen, Eigenschaften und Qualitätsstufen └─ Wasserstoff └─ Wasserstoff Feuerzeug
Wasserstoff
Wasserstoff ist das chemische Element mit dem Symbol H und der Ordnungszahl 1. Es ist das leichteste und häufigste Element im Universum. Unter Normalbedingungen ist Wasserstoff ein farb-, geruch- und geschmackloses Gas das als Molekül H₂ vorliegt.
Geschichte
Wasserstoff wurde 1766 von dem englischen Naturforscher Henry Cavendish als eigenständiges Element erkannt. Cavendish bezeichnete das Gas als "brennbare Luft" und stellte fest, dass es beim Verbrennen Wasser bildet.
Den Namen Hydrogenium, aus dem Griechischen hydro für Wasser und genes für Erzeuger, gab ihm 1787 der französische Chemiker Antoine Laurent de Lavoisier. Lavoisier bewies durch quantitative Versuche dass Wasser eine Verbindung aus Wasserstoff und Sauerstoff ist. Damit widerlegte er die Phlogistontheorie.
Bereits 1671 hatte Robert Boyle beim Auflösen von Eisen in Säuren ein brennbares Gas beobachtet, es aber nicht als neues Element erkannt.
Nutzung
Damalige Nutzung
- Ballonfahrt und Luftschiffe: Ab 1783 wurde Wasserstoff wegen seiner geringen Dichte als Traggas genutzt. Der erste Gasballon von Jacques Charles stieg mit Wasserstoff auf. Zeppeline verwendeten bis zum Hindenburg-Unglück 1937 Wasserstoff als Traggas.
- Knallgas: Das Gemisch aus Wasserstoff und Sauerstoff im Verhältnis 2:1 wurde als Knallgas für Beleuchtung und zum Schweißen genutzt. Drummondsches Licht verwendete eine Knallgasflamme.
- Reduktionsmittel: In der Metallurgie zur Reduktion von Metalloxiden.
- Laborchemie: Als Reagenz und zum Nachweis von Elementen.
Heutige Nutzung
- Ammoniaksynthese: Über 50 % der Weltproduktion gehen in das Haber-Bosch-Verfahren zur Düngerherstellung.
- Raffinerien: Zum Cracken von Kohlenwasserstoffen und zur Entschwefelung von Kraftstoffen.
- Methanolsynthese: Wasserstoff ist Grundstoff für Methanol, das weiter zu Formaldehyd und Kunststoffen verarbeitet wird.
- Lebensmittelindustrie: Zur Fetthärtung bei der Margarineherstellung.
- Energiespeicher: Als Speichermedium für überschüssigen Strom aus erneuerbaren Energien. Stichwort Power-to-Gas.
- Brennstoffzelle: In Fahrzeugen zur emissionsfreien Stromerzeugung. Nur Wasser als Abgas.
- Raketenantrieb: Flüssiger Wasserstoff als Treibstoff, z.B. bei der Ariane 5 oder dem Space Shuttle.
- Halbleiterindustrie: Als Schutzgas und Reduktionsmittel.
Herstellung
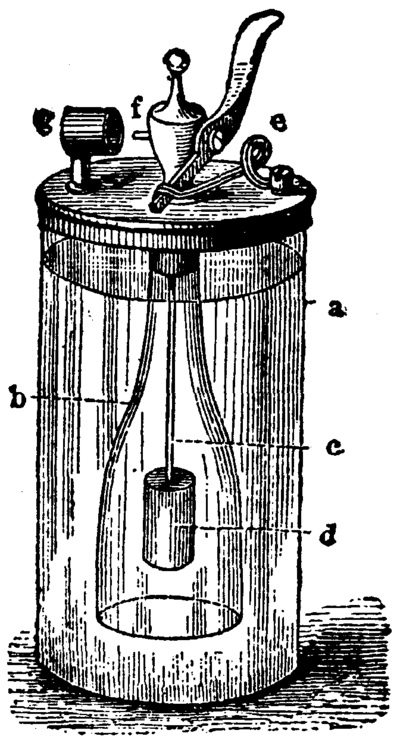
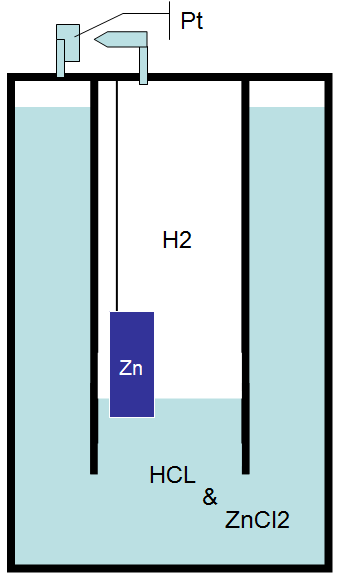
Schulexperiment: Salzsäure und Zink
Die einfachste Labormethode zur Erzeugung kleiner Mengen Wasserstoff:
Die Reaktionsgleichung: Zn + 2HCl = ZnCl_2 + H_2
Durchführung:
Zinkgranalien werden in einem Reagenzglas mit verdünnter Salzsäure übergossen. Sofort setzt eine Gasentwicklung ein. Das entstehende Gas kann in einem umgedrehten Reagenzglas aufgefangen werden. Die Knallgasprobe weist Wasserstoff nach: Es brennt mit einem pfeifenden Ton ab.
Diese chemische Reaktion, wurde für Wasserstoff Feuerzeuge bzw. Platinfeuerzeuge genutzt.
Zinkchlorid als Lötwasser:
Das Nebenprodukt Zinkchlorid ZnCl₂ ist stark hygroskopisch und in Wasser gelöst als Lötwasser bekannt. Es löst Oxidschichten von Metallen und ermöglicht es, auch Eisen, Stahl oder Edelstahl kalt mit Lötzinn zu löten. Ohne Lötwasser würde das Lot auf Eisen abperlen. Die Säure im Lötwasser beizt die Oberfläche metallisch blank.
Größere Mengen: Historisches Verfahren für Gasballone
Für die Füllung von Gasballonen im 18. und 19. Jahrhundert brauchte man Kilogramm-weise Wasserstoff. Das Laborverfahren war zu langsam.
Verfahren: Wasserdampf über Eisen
Wasserdampf wurde durch ein rotglühendes Eisenrohr oder über glühende Eisenspäne geleitet.
Die Reaktionsgleichung:
- <math>\mathrm{3\ Fe + 4\ H_2O \ \xrightarrow{500-800^\circ C} \ Fe_3O_4 + 4\ H_2 \uparrow}</math>
Ablauf:
1. Eisen wird im Ofen auf Rotglut von 500 bis 800 °C erhitzt.
2. Wasserdampf wird über das Eisen geleitet.
3. Das Eisen oxidiert zu Eisen(II,III)-oxid, auch Hammerschlag genannt.
4. Wasserstoff wird frei und kann abgeleitet werden.
5. Das Eisenoxid muss danach durch Reduktion mit Kohlenstoff wieder zu Eisen regeneriert werden.
Dieses Verfahren war gefährlich und energieaufwendig, lieferte aber die benötigten Mengen für die frühe Luftfahrt.
Heute: Industrielle Verfahren
1. Dampfreformierung von Erdgas:
Über 95 % des Wasserstoffs werden heute aus fossilen Quellen gewonnen. Erdgas reagiert mit Wasserdampf bei 700 bis 1000 °C an Nickel-Katalysatoren.
- <math>\mathrm{CH_4 + H_2O \rightarrow CO + 3\ H_2}</math>
- <math>\mathrm{CO + H_2O \rightarrow CO_2 + H_2}</math>
Nachteil: Es entsteht CO₂ als Nebenprodukt. Man spricht von "grauem Wasserstoff".
2. Elektrolyse von Wasser:
Die umweltfreundliche Alternative. Wasser wird mit elektrischem Strom in Wasserstoff und Sauerstoff zerlegt.
Die Reaktionsgleichung:
- <math>\mathrm{2\ H_2O \ \xrightarrow{Elektrolyse} \ 2\ H_2 \uparrow + O_2 \uparrow}</math>
Wird der Strom aus erneuerbaren Energien gewonnen, spricht man von grünem Wasserstoff. Er gilt als Schlüsseltechnologie der Energiewende.
Wasserstoff als Energiespeicher und Synthesegas:
1. Energiespeicher: Überschüssiger Wind- oder Solarstrom wird per Elektrolyse in Wasserstoff umgewandelt. Dieser kann gespeichert, transportiert und bei Bedarf in Brennstoffzellen wieder verstromt werden.
2. Synthesegas: Ein Gemisch aus Wasserstoff und Kohlenmonoxid ist Ausgangsstoff für die Fischer-Tropsch-Synthese zu synthetischen Kraftstoffen oder für die Methanolsynthese.
Sicherheit
Wasserstoff ist mit Luft im Bereich von 4 bis 77 Volumenprozent explosiv. Das Gemisch wird Knallgas genannt. Wasserstoff verflüchtigt sich wegen seiner geringen Dichte im Freien sehr schnell nach oben. In geschlossenen Räumen besteht Explosionsgefahr. Wasserstoffflammen sind bei Tageslicht kaum sichtbar.
Literatur
- August Wilhelm von Hofmann: Einleitung in die moderne Chemie. Vieweg, Braunschweig 1865.
- Henry Cavendish: Experiments on Factitious Air. Philosophical Transactions 1766.