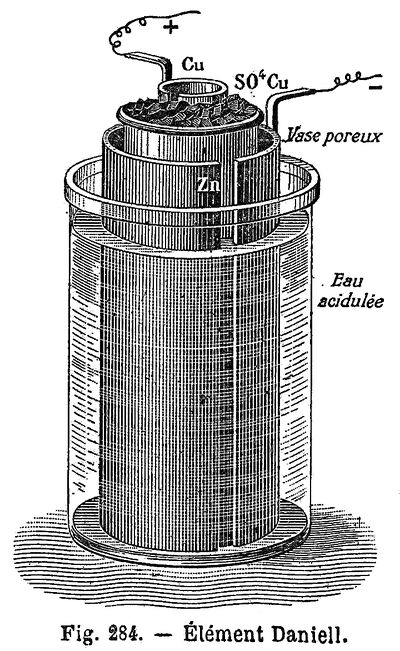
Daniell-Element
Inhaltsverzeichnis
Siehe:
Wie man Strom in Batterien speichert ├─ Natrium-Ionen-Akkumulatoren ├─ Edison Batterie ├─ Erdbatterie – Was wirklich dahintersteckt └─ Daniell-Element
Daniell-Element
Das Daniell-Element (auch Daniell-Zelle oder Daniell’sches Element genannt) ist eine der klassischsten und wichtigsten galvanischen Zellen (auch Volta’sche Zelle genannt). Es wurde 1836 von dem britischen Chemiker John Frederic Daniell erfunden und gilt als das erste zuverlässige und praktisch nutzbare galvanische Element, das eine konstante Spannung lieferte – im Gegensatz zur früheren Volta’schen Säule, die schnell „ermüdete“.
Es dient bis heute als Lehrbuch-Beispiel für die Funktionsweise einer galvanischen Zelle und erklärt perfekt, wie chemische Energie in elektrische Energie umgewandelt wird – genau wie bei der „Erdbatterie“ aus Kupfer und Zink, nur viel kontrollierter und effizienter.
Aufbau des Daniell-Elements
Es besteht aus zwei Halbzellen, die ionisch (nicht elektronisch) miteinander verbunden sind:
- Zink-Halbzelle (Anode – Minuspol)
- Elektrode: Zink-Stab oder Zink-Blech (oft amalgamiert, d. h. mit Quecksilber legiert, um Wasserstoff-Entwicklung zu verhindern)
- Elektrolyt: Zinksulfat-Lösung (ZnSO₄ aq, meist verdünnt)
- Kupfer-Halbzelle (Kathode – Pluspol)
- Elektrode: Kupfer-Stab oder Kupfer-Gefäß
- Elektrolyt: Kupfersulfat-Lösung (CuSO₄ aq, meist gesättigt oder konzentriert)
- Verbindung der Halbzellen
- Salzbrücke (Ionenbrücke): Ein mit gesättigter KCl-, KNO₃- oder Agar-Agar-Lösung getränkter Streifen (z. B. Filterpapier) oder eine poröse Scheidewand (historisch oft ein poröser Tontopf).
→ Ermöglicht Ionenwanderung (Ladungsausgleich), verhindert aber Vermischung der Lösungen.
- Äußerer Stromkreis
- Drahtverbindung zwischen Zink- und Kupfer-Elektrode (z. B. mit Voltmeter oder Verbraucher).
Historische Variante (Daniell original): Kupfer-Gefäß mit CuSO₄-Lösung, darin ein poröser Tontopf mit verdünnter H₂SO₄ + Zink-Elektrode.
Chemische Reaktionen – detailliert
Anode (Oxidation – Zink-Halbzelle, Minuspol): Zn(s) → Zn²⁺(aq) + 2 e⁻ → Zink-Atome lösen sich als Ionen auf und geben 2 Elektronen pro Atom ab. → Die Elektrode wird negativ (Elektronen-Überschuss).
Kathode (Reduktion – Kupfer-Halbzelle, Pluspol): Cu²⁺(aq) + 2 e⁻ → Cu(s) → Kupfer(II)-Ionen nehmen die Elektronen auf und scheiden sich als metallisches Kupfer an der Elektrode ab (rotbrauner Belag). → Die Elektrode wird positiv (Elektronen-Mangel).
Gesamtreaktion (Redox-Gleichung): Zn(s) + Cu²⁺(aq) → Zn²⁺(aq) + Cu(s)
Warum läuft die Reaktion genau so (und nicht umgekehrt)? Zink ist unedler als Kupfer (steht weiter links in der Spannungsreihe). Es hat eine stärkere Tendenz, Elektronen abzugeben (höhere Lösungstension). Kupfer ist edler und nimmt Elektronen leichter auf.
Standardpotential und Spannung
Unter Standardbedingungen (25 °C, 1 mol/L Konzentration, 1 bar):
- Standard-Reduktionspotential Kupfer: E°(Cu²⁺/Cu) = +0,34 V
- Standard-Reduktionspotential Zink: E°(Zn²⁺/Zn) = –0,76 V
Zellspannung (EMK = elektromotorische Kraft): E°Zelle = E°Kathode – E°Anode = +0,34 V – (–0,76 V) = +1,10 V (theoretisch genau 1,1018–1,10 V; in der Praxis oft 1,07–1,10 V je nach Konzentration).
Die positive Spannung zeigt: Die Reaktion läuft spontan in diese Richtung (ΔG < 0).
Ladungsausgleich durch die Salzbrücke
- An der Anode entstehen Zn²⁺ (positive Ladung im Elektrolyten).
- An der Kathode verschwinden Cu²⁺ (positive Ladung wird weniger).
→ Ohne Ausgleich würde sich die Zelle schnell polarisieren und stoppen. → Die Salzbrücke lässt Anionen (z. B. SO₄²⁻ oder Cl⁻) zur Anode wandern und Kationen (z. B. K⁺) zur Kathode → Ladungsneutralität bleibt erhalten.
Warum ist das Daniell-Element so wichtig?
- Erste stabile, praktisch nutzbare Batterie (vorher Volta-Säule: Spannung fiel schnell ab durch Polarisation).
- Zeigt klar: Galvanische Zellen nutzen spontane Redox-Reaktionen zwischen zwei unterschiedlich edlen Metallen.
- Direkte Vorläufer aller Batterien (Zink-Kohle, Alkaline, etc.).
- Erklärt exakt, warum die einfache „Erdbatterie“ (Kupfer + Zink im Boden) Strom liefert: Der Boden wirkt als Elektrolyt + Salzbrücke-Ersatz, aber unkontrolliert und schwach.
Kurz: Das Daniell-Element ist der Prototyp aller chemischen Batterien, bei denen ein unedles Metall (Zink) seine chemisch gebundene Energie abgibt, um Elektronen fließen zu lassen – genau das, was bei vielen YouTube-„Erdbatterien“ passiert, nur ohne die Kupfersulfat-Lösung und ohne Salzbrücke.