Branntkalk Calciumoxid
Inhaltsverzeichnis
- 1 Herstellen
- 2 Ab wann wurde Kalk gebrannt ?
- 3 Wozu wurde gebrannter Kalk neben Mörtel benötigt
- 4 Aufbau eines alten Kalkofens
- 5 Wo findet sich Kalk
- 6 Kalk brennen im Lagerfeuer
- 7 Was passiert beim Kalk löschen
- 8 Unterschied zwischen gebranntem Kalk und gelöschtem Kalk
- 9 Was passiert im Mörtel
- 10 Literatur
Herstellen
Der kleine Alchemist ├─ Branntkalk Calciumoxid └─ Wasserglas
Ab wann wurde Kalk gebrannt ?
Das Brennen von Kalkstein gehört zu den ältesten chemisch-technischen Verfahren der Menschheit. Archäologische Funde belegen die Nutzung von gebranntem Kalk bereits im Neolithikum, etwa ab 7000 v. Chr. in der Levante. In Çatalhöyük in der heutigen Türkei wurden Fußböden aus Kalkestrich nachgewiesen.
Systematisch genutzt wurde Kalk ab dem 3. Jahrtausend v. Chr. im Alten Ägypten und in Mesopotamien. Die Römer perfektionierten die Technik ab 300 v. Chr. mit großtechnischen Kalköfen. Vitruv beschreibt in De architectura im 1. Jh. v. Chr. detailliert das Kalkbrennen und die Mörtelherstellung. Römischer Opus caementicium wäre ohne gebrannten Kalk undenkbar gewesen.
In Mitteleuropa verbreitete sich das Kalkbrennen flächendeckend mit der Romanisierung ab dem 1. Jahrhundert n. Chr. Im Mittelalter war jeder größere Bauort mit einem oder mehreren Kalköfen ausgestattet. Bis zur Industrialisierung im 19. Jahrhundert wurde Kalk fast ausschließlich in Feldöfen und Grubenöfen gebrannt.
Wozu wurde gebrannter Kalk neben Mörtel benötigt
Gebrannter Kalk, chemisch Calciumoxid CaO, war ein universeller Grundstoff:
- Landwirtschaft: Zur Bodenverbesserung auf sauren Böden. Kalk neutralisiert Säuren, verbessert die Krümelstruktur und setzt Nährstoffe frei. Auch zur Desinfektion von Ställen.
- Ledergerbung: Beim Äschern wurden Tierhäute in Kalkbrühe eingelegt. Der Kalk löst Haare und Fettreste und quillt die Hautfasern auf.
- Zuckerindustrie: Zur Scheidung von Rübensaft. Kalk bindet Nichtzuckerstoffe die dann ausfallen.
- Eisenverhüttung: Als Zuschlagstoff im Hochofen. Kalk bindet die kieselsäurehaltige Gangart zu Schlacke.
- Seifensiederei: Zur Herstellung von Ätzkali aus Pottasche und Kalk. Grundlage für Schmierseife.
- Bauwesen: Neben Mörtel auch für Kalkanstriche, Tünche und Stuck. Kalkfarbe wirkt desinfizierend.
- Chemische Industrie: Ausgangsstoff für Calciumcarbid, Chlorkalk und Soda nach dem Solvay-Verfahren.
- Wasseraufbereitung: Zur Enthärtung und pH-Wert-Anhebung von Trinkwasser.
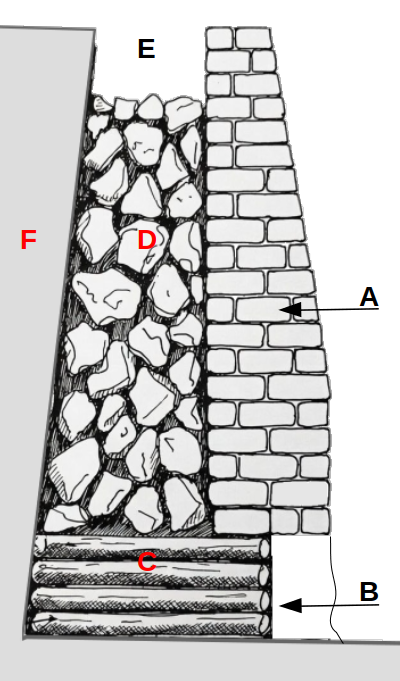
Aufbau eines alten Kalkofens
Der klassische Feldofen oder Grubenofen war die häufigste Bauform bis ins 19. Jahrhundert.
Die Größen Formen und Maße variierten je nach Ofen. Die angegebenen Maße sind nur Richtwerte.
A: Vordere Mauer: Bei Hangöfen die freistehende Mauer zur Talseite. Massive Bruchsteinmauer zur Stabilisierung und Wärmedämmung.
B: Schürloch: Öffnung an der Vorderseite, etwa 1 m breit und 0,7 m hoch. Diente zum Einbringen des Brennmaterials und zur Luftzufuhr. Oft mit Gewölbe gemauert.
C: Feuerraum / Schürraum: Raum direkt hinter dem Schürloch. Hier brannte das Holz, Torf oder später Kohle. Der Boden war meist gepflastert.
über "C": Gewölbe / Rost: Über dem Feuerraum wurde aus großen Kalksteinen ein falsches Gewölbe gesetzt. Die Zwischenräume ließen die heißen Gase durch, trugen aber das Brenngut.
D: Ofenschacht: Der eigentliche Brennraum. Zylindrisch oder leicht konisch nach oben zulaufend. Durchmesser 2 bis 4 m, Höhe 3 bis 6 m. Wände aus Bruchstein oder Ziegeln, oft in den gewachsenen Stein oder Hang gebaut.
in "D": Brenngut: Der Ofenschacht wurde schichtweise mit Kalksteinbrocken von Faust- bis Kopfgröße gefüllt. Faustregel: Je reiner der Kalkstein CaCO₃, desto besser der Branntkalk.
E: Gicht: Obere Öffnung des Ofens. Diente zum Befüllen und zum Abzug der Rauchgase. Wurde während des Brandes oft teilweise abgedeckt um Zug zu regulieren.
F: Wenn an einem Hang gebaut: gewachsener Fels
Ein Brand dauerte je nach Ofengröße 3 bis 7 Tage bei Temperaturen von 900 bis 1200 °C. Danach 2 bis 3 Tage Abkühlzeit.
Noch heute weisen Straßennamen oder Ortsbezeichnungen darauf hin das sich dort ein oder mehrere Brennöfen befunden haben.
"Am Kalkofen" oder ähnliche Bezeichnungen.
Wo findet sich Kalk
Calciumcarbonat CaCO₃ ist eines der häufigsten Minerale der Erdkruste. Natürliche Vorkommen:
- Gesteine: Kalkstein, Marmor, Kreide, Dolomit. Entstanden aus Ablagerungen von Kalkschalen fossiler Meerestiere. Ganze Gebirge wie die Schwäbische Alb oder die Dolomiten bestehen aus Kalk.
- Muschelschalen: Bestehen zu 95 % aus Calciumcarbonat in Form von Aragonit oder Calcit. Wurden historisch in Küstennähe direkt als Kalkrohstoff gebrannt.
- Schneckengehäuse: Ebenfalls hauptsächlich CaCO₃. In kalkarmen Regionen wurden Weinbergschneckenhäuser gesammelt und mitgebrannt.
- Eierschalen: Bestehen zu etwa 94 % aus Calciumcarbonat. Spielten technisch keine Rolle, demonstrieren aber das Prinzip. Hühner benötigen Kalk für die Schalenbildung.
- Knochen: Enthalten Calciumphosphat, nicht Calciumcarbonat. Werden daher nicht zu Branntkalk, sondern zu Knochenasche gebrannt.
- Korallen: Riffbildende Korallen bauen Skelette aus Aragonit. Korallenkalk wurde in tropischen Regionen genutzt.
Kalk brennen im Lagerfeuer
Was passiert in der Hitze ?
Beim Kalkbrennen läuft die thermische Dissoziation von Calciumcarbonat ab. Diese Reaktion ist endotherm, benötigt also ständige Wärmezufuhr.
Die Reaktionsgleichung: CaCO3 + Energie 900-1200 Grad Celsius = CaO + CO2
Im Detail:
- Ab 600 °C: Das Kristallwasser entweicht. Der Kalkstein wird porös.
- Ab 825 °C: Die Zersetzung beginnt an der Oberfläche. CO₂ entweicht.
- 900-1200 °C: Optimale Brenntemperatur. Das CO₂ muss zügig abziehen, sonst kehrt sich die Reaktion um. Die Reaktion frisst sich von außen nach innen durch den Stein.
- Über 1250 °C: Gefahr des Totbrennens. Der Branntkalk sintert, wird glasig hart und reagiert später nur sehr langsam mit Wasser.
Ein gut gebrannter Stein ist leicht, porös, weiß bis grau-weiß und zerfällt bei Wasserzugabe. Im Lagerfeuer werden diese Temperaturen nur im Glutkern erreicht. Das Ergebnis ist meist unvollständig gebrannt mit Kernen aus Kalkstein.
Was passiert beim Kalk löschen
Das Löschen ist eine heftig exotherme chemische Reaktion. Branntkalk CaO reagiert mit Wasser zu Calciumhydroxid Ca(OH)₂.
Die Reaktionsgleichung: CaO + H2O = Ca(OH)_2 + 64,8 \ kJ Wärmeenergie
Ablauf:
- Wasserzugabe: Wird Branntkalk mit Wasser übergossen, saugt er es begierig auf.
- Reaktion: Unter starkem Zischen und Dampfen erhitzt sich die Masse auf bis zu 300 °C. Es besteht Verbrühungsgefahr.
- Zerfall: Die kompakten Branntkalkstücke zerfallen zu feinem Pulver oder Brei. Das Volumen nimmt um das 2,5 bis 3,5-fache zu.
- Produkt: Je nach Wassermenge entsteht Kalkpulver bei wenig Wasser, Kalkbrei bei mittlerer Menge oder Kalkmilch bei Wasserüberschuss.
Achtung: Branntkalk ist stark ätzend. Staub und Spritzer verursachen schwere Verätzungen an Haut und Augen. Beim Löschen immer Schutzbrille und Handschuhe tragen.
Unterschied zwischen gebranntem Kalk und gelöschtem Kalk
| Eigenschaft | Gebrannter Kalk / Branntkalk | Gelöschter Kalk / Löschkalk |
|---|---|---|
| Chemische Formel | CaO | Ca(OH)₂ |
| Chemischer Name | Calciumoxid | Calciumhydroxid |
| Aggregatzustand | Feste, steinartige Brocken | Weißes Pulver oder Brei |
| Verhalten mit Wasser | Reagiert heftig exotherm | Bildet Suspension, kaum Reaktion |
| pH-Wert | 12,6 in gesättigter Lösung | 12,4 in gesättigter Lösung |
| Ätzwirkung | Stark ätzend, entzieht Gewebe Wasser | Ätzend, aber weniger aggressiv |
| Lagerung | Muss absolut trocken lagern. Zieht CO₂ und H₂O aus Luft | Luftdicht oder unter Wasser. Bindet CO₂ aus Luft ab |
| Anwendung | Rohstoff zum Löschen, Bodenkalk, Trocknungsmittel | Direkt als Mörtel, Anstrich, Dünger verwendbar |
Was passiert im Mörtel
Frisch angemachter Kalkmörtel besteht aus gelöschtem Kalk Ca(OH)₂, Sand und Wasser. Das Erhärten ist ein zweistufiger Prozess:
1. Physikalische Erhärtung: Das Anmachwasser verdunstet und wird vom Mauerwerk abgesaugt. Der Mörtel wird fest, ist aber noch nicht chemisch gebunden.
2. Chemische Erhärtung: Carbonatisierung: Der entscheidende Schritt. Das Calciumhydroxid nimmt Kohlendioxid aus der Luft auf und wandelt sich zurück zu Calciumcarbonat um.
Die Reaktionsgleichung: Ca(OH)2 + CO2 = CaCO3 + H_2O
Dabei gilt:
- Das entstehende Calciumcarbonat bildet feine Kristalle. Diese verfilzen sich mit den Sandkörnern und bilden ein festes Gefüge.
- Das freiwerdende Wasser verdunstet.
- Die Reaktion läuft sehr langsam von außen nach innen ab. Da CO₂ erst durch den Mörtel diffundieren muss, kann die vollständige Aushärtung je nach Mauerstärke Monate bis Jahre dauern.
- Das Endprodukt ist chemisch identisch mit dem Ausgangsstoff Kalkstein. Der Kreislauf CaCO₃ → CaO → Ca(OH)₂ → CaCO₃ hat sich geschlossen.
Deshalb heißt es: Kalkmörtel erhärtet durch Aufnahme von CO₂ aus der Luft. Er bindet nicht hydraulisch ab wie Zement, sondern carbonatisch.
Literatur
- Friedrich Schulte: Kalköfen und Kalkbrenner. Deutsches Museum, München 1984.
- Vitruv: De architectura libri decem, Buch II, Kapitel 5.